废糖蜜硫酸溶液中软锰矿的浸出动力学
用收缩芯模型研究了硫酸介质中废糖蜜还原浸出软锰矿的动力学,考察了软锰矿粒度、反应温度、浸出时间、硫酸浓度和废糖蜜浓度对锰浸出速率的影响。结果表明,提高反应温度、硫酸浓度、废糖蜜浓度和减小软锰矿颗粒的初始平均半径,均可以提高锰的浸出速率。废糖蜜还原浸出软锰矿属界面化学反应控制,表现活化能为45.6KJ/mol,硫酸和废糖蜜的反应级数分别为0.52和0.28.
关键词:软锰矿 废糖蜜 浸出 动力学
1 前 言
多年来,软锰矿直接还原浸出工艺的研究主要集中在使用无机还原剂,其特点是价廉易得。但在生产上存在渣量大、带入杂质多的缺点,如硫铁矿;或浸出液过滤困难,如硫酸亚铁;或副反应多,如SO2。因此,人们试图寻找有机物替代无机还原剂。研究表明,在酸性介质中使用醇类、酚类及芳胺类、草酸、蔗糖、葡萄糖等有机物还原剂,反应条件温和,锰的浸出率高,且不会带入无机杂质,所制产品纯度较高。但有机还原剂价格较高,从而限制了其在工业上的推广应用。废糖蜜是制糖过程的副产物,含有丰富的糖类等有机物,利用废糖蜜直接还原软锰矿浸出锰的条件温和、工业简单,锰浸出率高达95%以上,是一种来源丰富、无毒、价格低廉的生物质还原剂。
目前,软锰矿直接还原浸出过程的机理研究主要集中在无机还原剂方面,对于有机物还原浸出软锰矿机理的研究报道不多,且主要集中在单一有机物。如Furlanni等研究了葡萄糖还原浸出纯MnO2和锰矿的过程,并鉴别了葡萄糖被氧化的产物。如Beolchini等认为蔗糖浸出锰矿属界面反应控制,其浸出动力学可用变活化能的缩芯模型描述。Momade等研究了甲醇还原浸出二氧化锰矿物的动力学,认为反应在前面30min由甲醇的外扩散控制,30min后为产物层扩散控制。Veglio等采用改进的缩芯模型研究了在硫酸介质中乳糖还原浸出锰矿的动力学,获得了不同锰矿粒度下的动力学参数。张亚辉等对苯胺还原浸出大洋锰结核的机理进行了研究与验证。
然而,对于使用废糖蜜浸出软锰矿的反应过程,由于废糖蜜成分复杂,含蔗糖、还原糖、胶体及色素等物质,构成了由多种还原剂组成的反应体系,因此该过程是一个多组分相互作用的液-固相反应过程。目前还未见废糖蜜浸出软锰矿动力学的研究报道,且单一有机物浸出软锰矿动力学的研究结果,也不能直接用于多种还原剂共同作用的浸出结果,
由于软锰矿与废糖蜜中有机还原剂反应的最主要氧化产物是CO2,因此,本工作采用COD(化学耗氧量)表示废糖蜜中多种还原性有机物的还原能力,将废糖蜜中多种有机物相互作用浸出软锰矿的复杂过程简化为具有相通还原能力的单一组分的还原浸出过程,并用收缩芯模型研究了该过程的浸出动力学,确定了控制步骤和活化能,得到了描述浸出过程的动力学方程,研究结果可为该工艺的开发提供参考。
2 实 验
2.1 原料与还原剂
实验所用软锰矿取自八一锰矿,主要化学成分见表1.软锰矿的矿物学分析表明,主要金属矿物为软锰矿(MnO2)和赤铁矿(Fe2O3),脉石矿物主要是二氧化硅(SiO2)和高岭石[Al2Si2O5(OH)4]。软锰矿样品经破碎、研磨和筛分,得到颗粒半径分别为0.109-0.140,0.075-0.096,0.061-0.075,0.048-0.0055和0.038-0.045mm的5种矿样,其初始平均半径分别为0.065,0.0043,0.0034,0.026和0.021mm。所用硫酸为分析纯。所用废糖蜜含37.31%蔗糖,4.12%转化糖和7.52%胶体物质,废糖蜜的COD值为0.78/g。
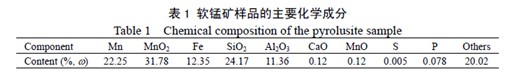
浸出动力学实验装置见图1.浸出试验在1000ml三口烧瓶中进行,置于恒温水浴中. 实验装置设有机械搅拌桨和变频无级调速. 温度计和取样器放置在一侧的开口中,冷凝器固定在另一侧的开口中以避免水分的蒸发。软锰矿矿物学分析采用Rigaku D/MAX2500 V型X射线衍射仪,COD测试采用XT-9900型智能微波消解仪,蔗糖含量测试采用AP IV589/880型旋仪。
2.3 动力学实验
首先加入废糖蜜和硫酸,在溶液温度达到设定值后,加入软锰矿,调节液固比,使溶液中固体矿物的浓度为10 g/L;定期取样进行分析. 实验表明,当搅拌速率提高到500 r/min 以上时,已消除外扩散对浸出过程的影响,因此,实验采用搅拌速率约为700 r/min.
2.4 分析方法
用硫酸亚铁铵滴定法分析滤液、浸渣和软锰矿的锰含量,并用式(1)计算锰的浸出率x(%),微波消解法测定COD,二次旋光法、兰艾农法和酒精凝聚法测定废糖蜜中蔗糖、还原糖和胶体的含量.
x=V(CMn-CMn0)/[m0(w0/54.94)]×100%. (1)
3 结果与讨论
3.1 废糖蜜中有机物还原浸出能力与COD值的关系
软锰矿中的MnO2不能被硫酸直接浸出,但由于MnO2在酸性条件下具有较强的氧化性,废糖蜜中的有机还原性物质在酸性介质中与MnO2发生氧化还原反应而水解和氧化,碳原子失去电子,由0 价变为+4 价,使软锰矿中的MnO2被还原为Mn2+而进入溶液中. 蔗糖与MnO2之间的化学反应为
24MnO2+C12H22O11+24H2SO4=24MnSO4+12CO2↑+35H2O. (2)
同理,废糖蜜中的含碳有机物与MnO2之间的氧化还原反应可用下式表示:
(C-HxOy)m+2mMnO2+2mH+→2mMn2++mCO2↑+zH2O. (3)
浸出过程中参与氧化还原反应的有机物总碳量nc与COD 消耗量mc的关系可表示为
nc=mc/32. (4)
由式(3)和(4)可知,锰的理论浸出量Ycal为
Ycal=3.43mc (5)
为确定有机物的还原浸出能力与COD 值的关系,设计了一组COD 消耗值与锰浸出量的实验. 浸出条件为废糖蜜浓度25.0 g/L,COD 19.1 g/L,废糖蜜与软锰矿质量比1:5,H2SO4 初始浓度1.88 mol/L. 不同浸出温度下浸出液COD 消耗量mc、锰的实际浸出量Yexp 和由式(5)计算的理论浸出量Ycal 如表2 所示.由表2 可知,当反应时间相同时,温度越高,COD消耗值越大,锰的浸出量也越大;温度相同时,COD消耗值和锰的浸出量随时间增加而增加. 拟合表2 中mc与Yexp 数据,可得如下直线关系:
Yexp=3.398mc (6)
相关系数R2 为0.93. 比较式(5), (6)和表2 数据可知,锰浸出量的实验值与用式(5)计算的理论值基本一致,说明用COD 值来表征废糖蜜中多组分有机物的还原能力是可行的. 因此,在下面的研究中用COD 值表示废糖蜜的浓度.
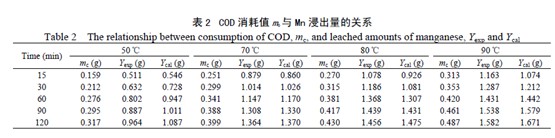
3.2 颗粒初始平均半径的影响
为了研究软锰矿粒径对锰浸出速率的影响,固定软锰矿用量5.0 g、反应温度80℃、硫酸浓度1.0 mol/L、废糖蜜COD 19.1 g/L,分别用不同初始平均半径的软锰矿颗粒进行浸出实验,结果见图2.从图2(a)可看出,锰浸出率随软锰矿颗粒初始平均半径减小而增加,说明软锰矿颗粒越小越易被浸出. 用不同控制步骤的收缩芯模型动力学方程处理图2(a)的数据,发现界面化学反应控制的动力学方程可较好地拟合实验数据:
1-(1-x)1/3={AMsCHpCMqexp[-Ea/(RT)]/(aρr0)}t=kt (7)
式中,AMsCHpCMqexp[-Ea/(RT)]/(aρr0). 式(7)反映了软锰矿颗粒初始平均半径、硫酸浓度、废糖蜜浓度和温度对反应的影响.不同粒径下1-(1-x)1/3与t 的关系见图2(b),5 条直线的相关系数R2均在0.95 以上. 从式(7)也可看出,减少软锰矿的初始平均半径r0,表观速率常数k 增加,从而导致锰的浸出速率随初始粒径下降而提高.
将图2(b)中不同初始平均半径所得直线的斜率kr与r0-1作图[见图2(c)],成直线关系,相关系数R2为0.99,进一步说明该浸出过程属界面化学反应控制.
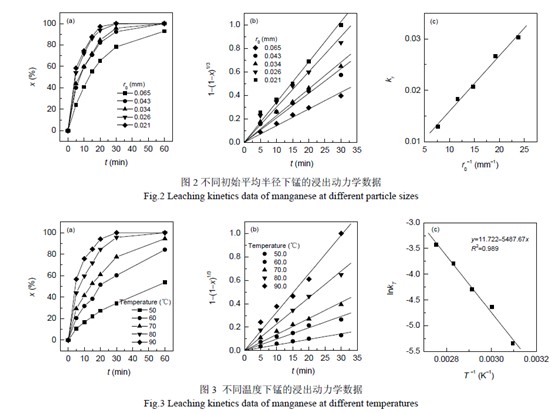
3.3 温度的影响
固定初始平均半径0.034 mm 的软锰矿用量5.0 g、硫酸浓度为1.0 mol/L、废糖蜜COD 19.1 g/L,研究了5个不同温度下软锰矿的浸出动力学,得到了相应的动力学数据. 图3(a)是不同温度下锰浸出率与时间的关系.用式(7)处理得到的锰浸出动力学数据均为直线关系[图3(b)],相关系数分别为 0.95(50.0℃), 0.95(60.0℃),0.97(70.0℃), 0.98(80.0℃)和 0.98(90.0℃),说明硫酸介质中废糖蜜浸出软锰矿的过程为界面化学反应控制. 由于随温度提高组分的扩散速率和化学反应速率均加快,所以锰的浸出速率随温度增加而增加.
由图3(b)得到不同温度下浸出反应的表观速率常数kT,将其代入阿仑尼乌斯方程的对数形式:
lnkT=lnA-Ea/(RT) (8)
用lnkT对T-1 作图,结果见图3(c). 拟合图3(c)数据可得
lnkT=11.722-5487.67T-1 (9)
相关系数R2=0.99. 综合式(8)和(9)可得到浸出过程的表观活化能Ea为45.6 kJ/mol.
3.4 硫酸浓度的影响
当初始平均半径0.034 mm 的软锰矿用量5.0 g、废糖蜜COD 19.1 g/L、反应温度80℃时,用不同浓度的硫酸浸出软锰矿,锰浸出率与时间的关系见图4(a),图4(b)是用式(7)处理图4(a)数据的结果.从图4 可知,锰浸出速率随硫酸初始浓度增加而增加,5 个不同硫酸初始浓度下1-(1-x)1/3 与t 成直线关系,相关系数R2分别为0.96(0.10 mol/L), 0.96(0.25 mol/L),0.98(0.50 mol/L), 0.98(1.00 mol/L)和0.96(1.50 mol/L),说明不同硫酸浓度下软锰矿的浸出过程可用界面化学反应控制的收缩芯模型描述.由图4(b)可求得各直线斜率,即浸出过程的表观速率常数k 分别为0.0069(0.10 mol/L), 0.0101(0.25 mol/L),0.0168(0.50 mol/L), 0.0226(1.00 mol/L)和0.0268(1.50mol/L). 假设表观速率常数与硫酸浓度的幂函数成正比,即
lnk=A+plnCH (10)
用式(10)拟合lnk和lnCH2SO4数据得
lnk=-3.083+0.52lnCH, (11)
相关系数R2=0.99. 可得硫酸的表观反应级数p 为0.52.
3.5 废糖蜜浓度的影响
固定初始平均半径0.0034mm的软锰矿用量5.0g、硫酸初始浓度为1.0mol/L、反应温度80℃,改变废糖蜜浓度进行实验,所得结果见图5.
图5(a)表明锰浸出率随废糖蜜浓度提高而增加,用式(7)处理图5(a)数据,得5条直线,相关系数R2分别为0.992(1.1g/L),0.984(4.1g/L),0.952(7.8g/L),0.953(15.0g/L),即界面化学反应控制的收缩芯模型可较好地描述不同浓度废糖蜜浸出软锰矿的动力学行为.
由图5(b)可得不同浓度废糖蜜还原浸出软锰矿的表观速率常数k(即各直线斜率). 假设表观速率常数与废糖蜜初始浓度CM 的幂函数成正比,即
lnk=B+qlnCM (12)
用式(12)处理不同废糖蜜浓度所得k 值,得
lnk=-4.69+0.28lnCM (13)
相关系数R2=0.958. 由式(12)和(13)可知废糖蜜的表观反应级数q 为0.28.
3.6 动力学方程及检验
将Ea=45.6 kJ/mol,p=0.52,q=0.28 代入式(7),用最小二乘法处理3.2-3.5 节的动力学数据,可得硫酸介质中废糖蜜浸出软锰矿的总动力程:
1-(1-x)1/3=(2033.7/r0)exp[-45.6×103/(RT)]CH
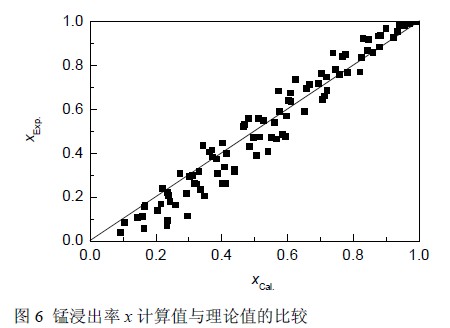
用式(14)验算不同实验条件下的动力学数据,并将计算值与实验值进行比较,结果见图6,计算值与实验值基本相符,偏差在10%左右. 因此,动力学方程(14)可较好地描述硫酸介质中废糖蜜还原浸出软锰矿的动力学行为. 该方程不仅可为研究废糖蜜中多组分有机物共同作用浸出软锰矿的动力学提供基础数据,也可为进一步优化浸出工艺提供理论指导.
4 结 论
通过实验研究了硫酸介质中废糖蜜浸出软锰矿的动力学,由研究结果得到如下主要结论:
(1)研究了硫酸浓度、废糖蜜浓度、软锰矿颗粒的初始平均半径和温度对锰浸出过程的影响,锰浸出速率随硫酸浓度、废糖蜜浓度和温度提高及软锰矿颗粒初始平均半径下降而增加.
(2)硫酸介质中废糖蜜浸出软锰矿受界面化学反应控制,表观活化能为45.6 kJ/mol,硫酸和废糖蜜的表观反应级数分别为0.52 及0.28.
(3)收缩芯模型界面化学反应控制方程可较好描述硫酸介质中废糖蜜还原浸出软锰矿的动力学,动力学方程为1-(1-x)1/3=(2033.7/r0)exp[-45.6×103/(RT)]CH

